Мировой рынок теллура. Теллур. Описание теллура. Свойства теллура Масса теллура
ОПРЕДЕЛЕНИЕ
Теллур расположен в пятом периоде VI группе главной (А) подгруппе Периодической таблицы.
Относится к элементам p -семейства. Металлоид. Обозначение - Te. Порядковый номер - 52. Относительная атомная масса - 127,60 а.е.м.
Электронное строение атома теллура
Атом теллура состоит из положительно заряженного ядра (+52), внутри которого есть 52 протона и 76 нейтронов, а вокруг, по пяти орбитам движутся 52 электрона.
Рис.1. Схематическое строение атома теллура.
Распределение электронов по орбиталям выглядит следующим образом:
52Te) 2) 8) 18) 18) 6 ;
1s 2 2s 2 2p 6 3s 2 3p 6 3d 10 4s 2 4p 6 4d 10 5s 2 5p 4 .
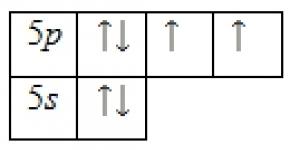
Внешний энергетический уровень атома теллура содержит 6 электронов, которые являются валентными. Энергетическая диаграмма основного состояния принимает следующий вид:

Валентные электроны атома теллура можно охарактеризовать набором из четырех квантовых чисел: n (главное квантовое), l (орбитальное), m l (магнитное) и s (спиновое):
|
Подуровень |
||||
Примеры решения задач
ПРИМЕР 1
Таким образом, для частиц S +6 , S 0 , S +4 и S -2 общее количество электронов в электронных оболочках будет равно 10, 16, 12 и 18, соответственно. Тогда, таблица примет следующий вид:
ПРИМЕР 2
Таким образом, для частиц C +4 , Al +3 , F и C 0 общее количество электронов в электронных оболочках будет равно 2, 10, 10 и 6, соответственно. Тогда, таблица примет следующий вид:
Вряд ли кто-либо поверит рассказу о капитане дальнего плавания, который, кроме того, профессиональный цирковой борец, известный металлург и врач-консультант хирургической клиники. В мире же химических элементов подобное разнообразие профессий - явление весьма распространенное, и к ним неприменимо выражение Козьмы Пруткова: «Специалист подобен флюсу: полнота его односторонняя». Вспомним (еще до разговора о главном объекте нашего рассказа) железо в машинах и железо в крови, железо - концентратор магнитного поля и железо - составную часть охры... Правда, на «профессиональную выучку» элементов порой уходило намного больше времени, чем на подготовку йога средней квалификации. Так и элемент № 52, о котором предстоит нам рассказать, долгие годы применяли лишь для того, чтобы продемонстрировать, каков он в действительности, этот элемент, названный в честь нашей планеты: «теллур» - от tellus, что по-латыни значит «Земля».
Открыт этот элемент почти два века назад. В 1782 г. горный инспектор Франц Йозеф Мюллер (впоследствии барон фон Рейхенштейн) исследовал золотоносную руду, найденную в Семигорье, на территории тогдашней Австро-Венгрии. Расшифровать состав руды оказалось настолько сложно, что ее назвали Aurum problematicum - «золото сомнительное». Именно из этого «золота» Мюллер выделил новый металл, но полной уверенности в том, что он действительно новый, не было. (Впоследствии оказалось, что Мюллер ошибался в другом: открытый им элемент был новым, но к числу металлов отнести его можно лишь с большой натяжкой.)
Чтобы рассеять сомнения, Мюллер обратился за помощью к видному специалисту, шведскому минералогу и химику-аналитику Бергману.
К сожалению, ученый умер, не успев закончить анализ присланного вещества - в те годы аналитические методы были уже достаточно точными, но анализ занимал очень много времени.
Элемент, открытый Мюллером, пытались изучать и другие ученые, однако лишь через 16 лет после его открытия Мартин Генрих Клапрот - один из крупнейших химиков того времени - неопровержимо доказал, что этот элемент на самом деле новый, и предложил для него название «теллур».
Как и всегда, вслед за открытием элемента начались поиски его применений. Видимо, исходя из старого, еще времен иатрохимии принципа - мир это аптека, француз Фурнье пробовал лечить теллуром некоторые тяжелые заболевания, в частности проказу. Но без успеха - лишь спустя много лет теллур смог оказать медикам некоторые «мелкие услуги». Точнее, не сам теллур, а соли теллуристой кислоты К 2 Те0 3 и Na 2 Te0 3 , которые стали использовать в микробиологии как красители, придающие определенную окраску изучаемым бактериям. Так, с помощью соединений теллура надежно выделяют из массы бактерий дифтерийную палочку. Если не в лечении, так хоть в диагностике элемент № 52 оказался полезен врачам.
Но иногда этот элемент, а в еще большей мере некоторые его соединения прибавляют врачам хлопот. Теллур Достаточно токсичен. В нашей стране предельно допустимой концентрацией теллура в воздухе считается 0,01 мг/м3. Из соединений теллура самое опасное - теллуроводород H 2 Те, бесцветный ядовитый газ с неприятным запахом. Последнее вполне естественно: теллур - аналог серы, значит, Н 2 Те должен быть подобен сероводороду. Он раздражает бронхи, вредно влияет на нервную систему.
Эти неприятные свойства не помешали теллуру выйти в технику, приобрести множество «профессий».
Металлурги интересуются теллуром потому, что уже небольшие его добавки к свинцу сильно повышают прочность и химическую стойкость этого важного металла. Свинец, легированный теллуром, применяют в кабельной и химической промышленности. Так, срок службы аппаратов сернокислотного производства, покрытых изнутри свинцово-теллуровым сплавом (до 0,5% Те), вдвое больше, чем у таких же аппаратов, облицованных просто свинцом. Присадка теллура к меди и стали облегчает их механическую обработку.
В стекольном производстве теллуром пользуются, чтобы придать стеклу коричневую окраску и больший коэффициент лучепреломления. В резиновой промышленности его, как аналог серы, иногда применяют для вулканизации каучуков.
Теллур - полупроводник
Однако не эти отрасли были виновниками скачка в ценах и спросе на элемент № 52. Произошел этот скачок в начале 60-х годов нашего века. Теллур - типичный полупроводник, и полупроводник технологичный. В отличие от германия и кремния, он сравнительно легко плавится (температура плавления 449,8° С) и испаряется (закипает при температуре чуть ниже 1000° С). Из него, следовательно, легко получать тонкие полупроводниковые пленки, которыми особенно интересуется современная микроэлектроника.
Однако чистый теллур как полупроводник применяют ограниченно - для изготовления полевых транзисторов некоторых типов и в приборах, которыми меряют интенсивность гамма-излучения. Да еще примесь теллура умышленно вводят в арсенид галлия (третий по значению после кремния и германия полупроводник), чтобы создать в нем проводимость электронного типа.
Намного обширнее область применения некоторых теллуридов - соединений теллура с металлами. Теллуриды висмута Bi 2 Te 3 и сурьмы Sb 2 Te 3 стали самыми важными материалами для термоэлектрических генераторов. Чтобы объяснить, почему это произошло, сделаем небольшое отступление в область физики и истории.
Еще полтора века назад (в 1821 г.) немецкий физик Зеебек обнаружил, что в замкнутой электрической цепи, состоящей из разных материалов, контакты между которыми находятся при разной температуре, создается электродвижущая сила (ее называют термо-ЭДС). Через 12 лет швейцарец Пельтье обнаружил эффект, обратный эффекту Зеебека: когда электрический ток течет по цепи, составленной из разных материалов, в местах контактов, кроме обычной джоулевой теплоты, выделяется или поглощается (в зависимости от направления тока) некоторое количество тепла.
Примерно 100 лет эти открытия оставались «вещью в себе», любопытными фактами, не более. И не будет преувеличением утверждать, что новая жизнь обоих этих эффектов началась после того, как академик А. Ф. Иоффе с сотрудниками разработал теорию применения полупроводниковых материалов для изготовления термоэлементов. А вскоре эта теория воплотилась в реальные термоэлектрогенераторы и термоэлектрохолодильники различного назначения.
В частности, термоэлектрогенераторы, в которых использованы теллуриды висмута, свинца и сурьмы, дают энергию искусственным спутникам Земли, навигационно - метеорологическим установкам, устройствам катодной защиты магистральных трубопроводов. Те же материалы помогают поддержать нужную температуру во многих электронных и микроэлектронных устройствах.
В последние годы большой интерес вызывает еще одно химическое соединение теллура, обладающее полупроводниковыми свойствами,- теллурид кадмия CdTe. Этот материал используют для изготовления солнечных батарей, лазеров, фотосопротнвлений, счетчиков радиоактивных излучений. Теллурид кадмия знаменит и тем, что это один из немногих полупроводников, в которых заметно проявляется эффект Гана.
Суть последнего заключается в том, что уже само введение маленькой пластинки соответствующего полупроводника в достаточно сильное электрическое поле приводит к генерации высокочастотного радиоизлучения. Эффект Гана уже нашел применение в радиолокационной технике.
Заключая, можно сказать, что количественно главная «профессия» теллура - легирование свинца и других металлов. Качественно же главное, безусловно, это работа теллура и теллуридов как полупроводников.
Полезная примесь
В таблице Менделеева место теллура находится в главной подгруппе VI группы рядом с серой и селеном. Эти три элемента сходны по химическим свойствам и часто сопутствуют друг другу в природе. Но доля серы в земной коре - 0,03%, селена всего - 10-5 %, теллура же еще на порядок меньше - 10~6%. Естественно, что теллур, как и селен, чаще всего встречается в природных соединениях серы - как примесь. Бывает, правда (вспомните о минерале, в котором открыли теллур), что он контактирует с золотом , серебром , медью и другими элементами. На нашей планете открыто более 110 месторождений сорока минералов теллура. Но добывают его всегда заодно или с селеном, или с золотом, или с другими металлами.
В России известны медно-никелевые теллурсодержащие руды Печенги и Мончегорска, теллурсодержащие свинцово-цинковые руды Алтая и еще ряд месторождений.
Из медной руды теллур выделяют на стадии очистки черновой меди электролизом. На дно электролизера вьпадает осадок - шлам. Это очень дорогой полупродукт. Приведем для иллюстрации состав шлама одного из канадских заводов: 49,8% меди, 1,976% золота, 10,52% серебра, 28,42% селена и 3,83% теллура. Все эти ценнейшие компоненты шлама надо разделить, и для этого существует несколько способов. Вот один из них.
Шлам расплавляют в печи, и через расплав пропускают воздух. Металлы, кроме золота и серебра, окисляются, переходят в шлак. Селен и теллур тоже окисляются, но - в летучие окислы, которые улавливают в специальных аппаратах (скрубберах), затем растворяют и превращают в кислоты - селенистую Н 2 SeОз и теллуристую Н 2 ТеОз. Если через этот раствор пропустить сернистый газ S0 2 , произойдут реакции
H 2 Se0 3 + 2S0 2 + Н 2 0 → Se ↓ + 2H 2 S0 4 .
H2Te03 + 2S02 + Н20 → Те ↓ + 2H 2 S0 4 .
Теллур и селен выпадают одновременно, чтo весьма не-желательно - они нужны нам порознь. Поэтому условия процесса подбирают таким образом, чтобы в соответствии с законами химической термодинамики сначала восстанавливался преимущественно селен. Этому помогает подбор оптимальной концентрации добавляемой в раствор соляной кислоты.
Затем осаждают теллур. Выпавший серый порошок, разумеется, содержит некоторое количество селена и, кроме того, серу, свинец, медь, натрий, кремний, алюминий, железо, олово, сурьму, висмут, серебро, магний, золото, мышьяк, хлор. От всех этих элементов теллур приходится очищать сначала химическими методами, затем перегонкой или зонной плавкой. Естественно, что из разных руд теллур извлекают по-разному.
Теллур вреден
Теллур применяют все шире и, значит, все возрастает число работающих с ним. В первой части рассказа об эле-менте № 52 мы уже упоминали о токсичности теллура и его соединений. Расскажем об этом подробней - именно потому, что с теллуром приходится работать все большему числу людей. Вот цитата из диссертации, посвященной теллуру как промышленному яду: белые крысы, которым ввели аэрозоль теллура, «проявляли беспокойство, чихали, терли мордочки, делались вялыми и сонливыми». Подобным образом действует теллур и на людей.
И сам теллур и его соединения могут приносить беды разных «калибров». Они, например, вызывают облысение, влияют на состав крови, могут блокировать различные ферментные системы. Симптомы хронического отравления элементарным теллуром - тошнота, сонливость, исхудание; выдыхаемый воздух приобретает скверный чесночный запах алкилтеллуридов.
При острых отравлениях теллуром вводят внутривенно сыворотку с глюкозой , а иногда даже морфий. Как профилактическое средство употребляют аскорбиновую кислоту. Но главная профилактика - это надежная герметизация аппаратов, автоматизация процессов, в которых участвуют теллур и его соединения.

Элемент № 52 приносит много пользы и уже потому заслуживает внимания. Но работа с ним требует осторожности, четкости и опять-таки - сосредоточенного внимания.
ВНЕШНИЙ ВИД ТЕЛЛУРА. Кристаллический теллур больше всего похож на сурьму. Цвет его - серебристо-белый. Кристаллы - гексагональные, атомы в них образуют спиральные цепи и связаны ковалентными связями с ближайшими соседями. Поэтому элементарный теллур можно считать неорганическим полимером. Кристаллическому теллуру свойствен металлический блеск, хотя по комплексу химических свойств его скорее можно отнести к неметаллам. Теллур хрупок, его довольно просто превратить в порошок. Вопрос о существовании аморфной модификации теллура однозначно не решен. При восстановлении теллура из теллуристой или теллуровой кислот выпадает осадок, однако до сих пор не ясно, являются ли эти частички истинно аморфными или это просто очень мелкие кристаллы.
ДВУХЦВЕТНЫЙ АНГИДРИД. Как и положено аналогу серы, теллур проявляет валентности 2-, 4+ и 6+ и значительно реже 2+. Моноокись теллура ТеО может существовать лишь в газообразном виде и легко окисляется до Те0 2 . Это белое негигроскопичное, вполне устойчивое кристаллическое вещество, плавящееся без разложения при 733° С; оно имеет полимерное строение.
В воде двуокись теллура почти не растворяется - в раствор переходит лишь одна часть Те0 2 на 1,5 млн. частей воды и образуется раствор слабой теллуристой кислоты Н 2 Те0 3 ничтожной концентрации. Так же слабо выражены кислотные свойства и у теллуровой кислоты
H 6 TeO 6 . Эту формулу (а не Н 2 ТеО 4 ей присвоили после того, как были получены соли состава Ag 6 Te0 6 и Hg 3 Te0 6 , хорошо растворяющиеся в воде. Образующий теллуровую кислоту ангидрид ТеОз в воде практически не растворяется. Это вещество существует в двух модификациях - желтого и серого цвета: α-ТеОз и β-ТеОз. Серый теллуровый ангидрид очень устойчив: даже при нагревании на него не действуют "кислоты и концентрированные щелочи. От желтой разновидности его очищают, кипятя смесь в концентрированном едком кали.
ВТОРОЕ ИСКЛЮЧЕНИЕ. При создании периодической таблицы Менделеев поставил теллур и соседний с ним иод (так же, как аргон и калий) в VI и VII группы не в соответствии, а вопреки их атомным весам. Действительно, атомная масса теллура - 127,61, а иода - 126,91 Значит, иод должен был бы стоять не за теллуром, а впереди него. Менделеев, однако, не сомневался в пра
вильности своих рассуждений, так как считал, что атомные веса этих элементов определены недостаточно точно. Близкий друг Менделеева чешский химик Богуслав Браунер тщательно проверил атомные веса теллура и иода, но его данные совпали с прежними. Правомерность исключений, подтверждающих правило, была установлена лишь тогда, когда в основу периодической системы легли не атомные веса, а заряды ядер, когда стал известен изотопный состав обоих элементов. У теллура, в отличие от иода, преобладают тяжелые изотопы.
Кстати, об изотонах. Сейчас известно 22 изотопа элемента № 52. Восемь из них - с массовыми числами 120, 122, 123, 124, 125, 126, 128 и 130 - стабильны. Последние два изотопа - самые распространенные: 31,79 и 34,48% соответственно.
МИНЕРАЛЫ ТЕЛЛУРА. Хотя теллура на Земле значительно меньше, чем селена, известно больше минералов элемента № 52, чем минералов его аналога. По своему составу минералы теллура двояки: или теллуриды, или продукты окисления теллуридов в земной коре. В числе первых калаверит AuTe 2 и креннерит (Au, Ag) Те2, входящие в число немногих природных соединений золота. Известны также природные теллуриды висмута, свинца, ртути. Очень редко в природе встречается самородный теллур. Еще до открытия этого элемента его иногда находили в сульфидных рудах, но не могли правильно идентифицировать. Практического значения минералы теллура не имеют - весь промышленный теллур является попутным продуктом переработки руд других металлов.
|
теллур элемент, теллур википедия
Теллу́р / Tellurium (Te), 52
(молярная масса)
127,60(3) а. е. м. (г/моль)
(+6e) 56 211 (−2e) пм
2,1 (шкала Полинга)
6, +4 , +2, −2
(первый электрон)
869,0 (9,01) кДж/моль (эВ)
17,91 кДж/моль
49,8 кДж/моль
25,8 Дж/(K·моль)
20,5 см³/моль
гексагональная
(300 K) 14,3 Вт/(м·К)
| 52 | |
| Te 127,60 | |
| 4d105s25p4 | |
Теллу́р
- химический элемент 16-й группы (по устаревшей классификации - главной подгруппы VI группы, халькогены), 5-го периода в периодической системе, имеет атомный номер 52; обозначается символом Te
(лат. Tellurium), относится к семейству металлоидов.
- 1 История
- 2 Происхождение названия
- 3 Нахождение в природе
- 3.1 Типы месторождений
- 4 Получение
- 4.1 Цены
- 5 Физические свойства
- 6 Химические свойства
- 7 Изотопы
- 8 Применение
- 8.1 Сплавы
- 8.2 Термоэлектрические материалы
- 8.3 Узкозонные полупроводники
- 8.4 Высокотемпературная сверхпроводимость
- 8.5 Производство резины
- 8.6 Производство халькогенидных стёкол
- 8.7 Источники света
- 8.8 CD-RW
- 9 Биологическая роль
- 9.1 Физиологическое действие
- 10 Примечания
- 11 Ссылки
История
Впервые был найден в 1782 году в золотоносных рудах Трансильвании горным инспектором Францем Йозефом Мюллером (впоследствии барон фон Райхенштейн), на территории Австро-Венгрии. 1798 году Мартин Генрих Клапрот выделил теллур и определил важнейшие его свойства.
Происхождение названия
От латинского tellus, родительный падеж telluris, Земля.
Нахождение в природе
Содержание в земной коре 1·10−6% по массе. Известно около 100 минералов теллура. Наиболее часты теллуриды меди, свинца, цинка, серебра и золота. Изоморфная примесь теллура наблюдается во многих сульфидах, однако изоморфизм Te - S выражен хуже, чем в ряду Se - S, и в сульфиды входит ограниченная примесь теллура. Среди минералов теллура особое значение имеют алтаит (PbTe), сильванит (AgAuTe4), калаверит (AuTe2), гессит (Ag2Te), креннерит, петцит (Ag3AuTe2), мутманнит, монбрейит (Au2Te3), нагиагит (4S5), тетрадимит (Bi2Te2S). Встречаются кислородные соединения теллура, например, ТеО2 - теллуровая охра.
Встречается самородный теллур и вместе с селеном и серой (японская теллуристая сера содержит 0,17 % Те и 0,06 % Se).
Типы месторождений
Большая часть упомянутых минералов развита в низкотемпературных золото-серебряных месторождениях, где они обычно выделяются после основной массы сульфидов совместно с самородным золотом, сульфосолями серебра, свинца, а также с минералами висмута. Несмотря на развитие большого числа теллуровых минералов, главная масса теллура, извлекаемого промышленностью, входит в состав сульфидов других металлов. частности, теллур в несколько меньшей степени, чем селен, входит в состав халькопирита медно-никелевых месторождений магматического происхождения, а также халькопирита, развитого в медноколчеданных гидротермальных месторождениях. Теллур находится также в составе пирита, халькопирита, молибденита и галенита месторождений порфировых медных руд, полиметаллических месторождений алтайского типа, галенита свинцово-цинковых месторождений, связанных со скарнами, сульфидно-кобальтовых, сурьмяно-ртутных и некоторых других. Содержание теллура в молибдените колеблется в пределах 8-53 г/т, в халькопирите 9-31 г/т, в пирите - до 70 г/т.
Получение
Основной источник - шламы электролитического рафинирования меди и свинца. Шламы подвергают обжигу, теллур остается в огарке, который промывают соляной кислотой. Из полученного солянокислого раствора теллур выделяют, пропуская через него сернистый газ SO2.
Для разделения селена и теллура добавляют серную кислоту. При этом выпадает диоксид теллура ТеО2, а H2SeO3 остается в растворе.
Из оксида ТеО2 теллур восстанавливают углем.
Для очистки теллура от серы и селена используют его способность под действием восстановителя (Al, Zn) в щелочной среде переходить в растворимый дителлурид динатрия Na2Te2:
Для осаждения теллура через раствор пропускают воздух или кислород:
Для получения теллура особой чистоты его хлорируют
Образующийся тетрахлорид очищают дистилляцией или ректификацией. Затем тетрахлорид гидролизуют водой:
,а образовавшийся ТеО2 восстанавливают водородом:
Цены
Теллур - редкий элемент, и значительный спрос при малом объёме добычи определяет высокую его цену (около $200–300 за кг в зависимости от чистоты), но, несмотря на это, диапазон областей его применения постоянно расширяется.
Физические свойства
Теллур - хрупкое серебристо-белое вещество с металлическим блеском. тонких слоях на просвет красно-коричневый, в парах - золотисто-жёлтый. При нагревании приобретает пластичность. Кристаллическая решётка - гексагональная. Коэффициент теплового расширения - 1,68·10-5 K−1. Диамагнетик. Полупроводник с шириной запрещённой зоны 0,34 эВ, тип проводимости - p в нормальных условиях и при повышенной температуре, n - при пониженной температуре (граница перехода - от минус 80 до минус 100 °C в зависимости от чистоты).
Химические свойства
В химических соединениях теллур проявляет степени окисления –2; +2; +4; +6. Является аналогом серы и селена, но химически менее активен, чем сера. Растворяется в щелочах, поддается действию азотной и серной кислот, но в разбавленной соляной кислоте растворяется слабо. С водой металлический теллур начинает реагировать при 100 °C.
С кислородом образует соединения TeO, TeO2, TeO3. виде порошка окисляется на воздухе даже при комнатной температуре, образуя оксид TeO2. При нагреве на воздухе сгорает, образуя TeO2 - прочное соединение, обладающее меньшей летучестью, чем сам теллур. Это свойство используется для очистки теллура от оксидов, которые восстанавливают проточным водородом при температуре 500-600 °C. Диоксид теллура плохо растворим в воде, хорошо - в кислых и щелочных растворах.
В расплавленном состоянии теллур довольно инертен, поэтому в качестве контейнерных материалов при его плавке применяют графит и кварц.
Теллур образует соединение с водородом при нагревании, легко реагирует с галогенами, взаимодествует с серой и фосфором и металлами. При взаимодействии с концентрированной серной кислотой образует сульфит. Образует слабые кислоты: теллурводородную (H2Te), теллуристую (H2TeO3) и теллуровую (H6TeO6), большинство солей которых плохо растворимы в воде.
Изотопы
Основная статья: Изотопы теллураИзвестны 38 нуклидов и 18 ядерных изомеров теллура с атомными числами от 105 до 142. Теллур - самый лёгкий элемент, чьи известные изотопы подвержены альфа-распаду (изотопы от 106Te до 110Te). Атомная масса теллура (127,60 г/моль) превышает атомную массу следующего за ним элемента - иода (126,90 г/моль).
В природе встречается восемь изотопов теллура. Шесть из них, 120Te, 122Te, 123Te, 124Te, 125Te и 126Te - стабильны. Остальные два - 128Te и 130Te - радиоактивны, оба они испытывают двойной бета-распад, превращаясь в изотопы ксенона 128Xe и 130Xe, соответственно. Стабильные изотопы составляют лишь 33,3 % от общего количества теллура, встречающегося в природе, что является возможным благодаря чрезвычайно долгим периодам полураспада природных радиоактивных изотопов. Они составляют от 7,9·1020 до 2,2·1024 лет. Изотоп 128Te имеет самый долгий подтверждённый период полураспада из всех радионуклидов - 2,2·1024 лет или 2,2 септиллиона лет, что примерно в 160 триллионов раз больше оценочного возраста Вселенной.
Применение
Сплавы
Теллур применяется в производстве сплавов свинца с повышенной пластичностью и прочностью (применяемых, например, при производстве кабелей). При введении 0,05 % теллура потери свинца на растворение под воздействием серной кислоты снижаются в 10 раз, и это используется при производстве свинцово-кислотных аккумуляторов. Так же важно то обстоятельство, что легированный теллуром свинец при обработке пластической деформацией не разупрочняется, и это позволяет вести технологию изготовления токоотводов аккумуляторных пластин методом холодной высечки и значительно увеличить срок службы и удельные характеристики аккумулятора.
Термоэлектрические материалы
Монокристалл теллурида висмутаТакже велика его роль в производстве полупроводниковых материалов и, в частности, теллуридов свинца, висмута, сурьмы, цезия. Очень важное значение в ближайшие годы приобретёт производство теллуридов лантаноидов, их сплавов и сплавов с селенидами металлов для производства термоэлектрогенераторов с весьма высоким (до 72-78 %) КПД, что позволит применить их в энергетике и в автомобильной промышленности.
Так, например, недавно обнаружена очень высокая термо-ЭДС в теллуриде марганца (500 мкВ/К) и в его сочетании с селенидами висмута, сурьмы и лантаноидов, что позволяет не только достичь весьма высокого КПД в термогенераторах, но и осуществить уже в одной ступени полупроводникового холодильника охлаждение вплоть до области криогенных (температурный уровень жидкого азота) температур и даже ниже. Лучшим материалом на основе теллура для производства полупроводниковых холодильников в последние годы явился сплав теллура, висмута и цезия, который позволил получить рекордное охлаждение до −237 °C. то же время, как термоэлектрический материал, перспективен сплав теллур-селен (70 % селена), который имеет коэффициент термо-ЭДС около 1200 мкВ/К.
Узкозонные полупроводники
Совершенно исключительное значение также получили сплавы КРТ (кадмий-ртуть-теллур), которые обладают фантастическими характеристиками для обнаружения излучения от стартов ракет и наблюдения за противником из космоса через атмосферные окна (не имеет значение облачность). КРТ является одним из наиболее дорогих материалов в современной электронной промышленности.
Высокотемпературная сверхпроводимость
Ряд систем, имеющих в своем составе теллур, недавно обнаружили существование в них трёх (возможно, четырёх) фаз, сверхпроводимость в которых не исчезает при температуре несколько выше температуры кипения жидкого азота.
Производство резины
Отдельной областью применения теллура является его использование в процессе вулканизации каучука.
Производство халькогенидных стёкол
Теллур используется при варке специальных марок стекла (где он применяется в виде диоксида), специальные стёкла, легированные редкоземельными металлами, применяются в качестве активных тел оптических квантовых генераторов.
Кроме того, некоторые стёкла на основе теллура являются полупроводниками, это свойство находит применение в электронике.
Специальные сорта теллурового стекла (достоинство таких стёкол - прозрачность, легкоплавкость и электропроводность), применяются в конструировании специальной химической аппаратуры (реакторов).
Источники света
Ограниченное применение теллур находит для производства ламп с его парами - они имеют спектр, очень близкий к солнечному.
CD-RW
Сплав теллура применяется в перезаписываемых компакт-дисках (в частности, фирмы Mitsubishi Chemical Corporation марки «Verbatim») для создания деформируемого отражающего слоя.
Биологическая роль
Микроколичества теллура всегда содержатся в живых организмах, его биологическая роль не выяснена.
Физиологическое действие
Теллур и его летучие соединения токсичны. Попадание в организм вызывает тошноту, бронхиты, пневмонию. ПДК в воздухе колеблется для различных соединений 0,007-0,01 мг/м³, в воде 0,001-0,01 мг/л. Канцерогенность теллура не подтверждена.
В целом соединения теллура менее токсичны, чем соединения селена.
При отравлениях теллур выводится из организма в виде отвратительно пахнущих летучих теллурорганических соединений - алкилтеллуридов, в основном диметилтеллурида (CH3)2Te. Их запах напоминает запах чеснока, поэтому при попадании в организм даже малых количеств теллура выдыхаемый человеком воздух приобретает этот запах, что является важным симптомом отравления теллуром.
Примечания
- Michael E. Wieser, Norman Holden, Tyler B. Coplen, John K. Böhlke, Michael Berglund, Willi A. Brand, Paul De Bièvre, Manfred Gröning, Robert D. Loss, Juris Meija, Takafumi Hirata, Thomas Prohaska, Ronny Schoenberg, Glenda O’Connor, Thomas Walczyk, Shige Yoneda, Xiang‑Kun Zhu. Atomic weights of the elements 2011 (IUPAC Technical Report) (англ.) // Pure and Applied Chemistry. - 2013. - Vol. 85, no. 5. - P. 1047-1078. - DOI:10.1351/PAC-REP-13-03-02.
- Tellurium: electronegativities (англ.). WebElements. Проверено 5 августа 2010.
- Leddicotte, G. W. (1961), «The radiochemistry of tellurium», Nuclear science series, Subcommittee on Radiochemistry, National Academy of Sciences-National Research Council, с. 5,
- Редкол.:Зефиров Н. С. (гл. ред.). Химическая энциклопедия: в 5 т. - Москва: Советская энциклопедия, 1995. - Т. 4. - С. 514. - 639 с. - 20 000 экз. - ISBN 5-85270-039-8.
- WebElements Periodic Table of the Elements | Tellurium | crystal structures
- Глинка Н. Л. Общая химия. - М.: «Химия», 1977, переработанное. - С. 395. - 720 с.
- 1 2 3 4 Теллур - статья из Большой советской энциклопедии
- 1 2 G. Audi, O. Bersillon, J. Blachot and A. H. Wapstra (2003). «The NUBASE evaluation of nuclear and decay properties». Nuclear Physics A 729 : 3–128. DOI:10.1016/j.nuclphysa.2003.11.001. Bibcode: 2003NuPhA.729....3A.
- Изотоп теллур-123 считался радиоактивным (β−-активным с периодом полураспада 6·1014 лет), однако после дополнительных измерений он был признан стабильным в пределах чувствительности эксперимента.
- 2,2 квадриллиона лет - по длинной шкале.
- Tellurium. International Programme on Chemical Safety (28 января 1998). Проверено 12 января 2007. Архивировано из первоисточника 4 августа 2012.
- Wright, PL (1966). «Comparative metabolism of selenium and tellurium in sheep and swine». AJP – Legacy 211 (1): 6–10. PMID 5911055.
- (1989) «Tellurium-intoxication». Klinische Wochenschrift 67 (22): 1152–5. DOI:10.1007/BF01726117. PMID 2586020.
- Taylor, Andrew (1996). «Biochemistry of tellurium». Biological Trace Element Research 55 (3): 231–239. DOI:10.1007/BF02785282. PMID 9096851.
Ссылки
- Теллур на Webelements
- Теллур в Популярной библиотеке химических элементов
| Соединения теллура | |
|---|---|
|
Гексафторид теллура (TeF6) Диоксид теллура (TeO2) Ортотеллурат натрия (Na6TeO6) Теллурат аммония ((NH4)2TeO4) Теллурид бериллия (BeTe) Теллурид висмута(III) (Bi2Te3) Теллурид дикалия (K2Te) Теллурид кадмия (CdTe) Теллурид натрия (Na2Te) Теллурид олова (SnTe) Теллурид ртути (HgTe) Теллурид свинца (PbTe) Теллурид цинка (ZnTe) Теллурит калия (K2TeO3) Теллурит натрия (Na2TeO3) Теллуровая кислота (H2TeO4 2H2O) Теллуроводород (H2Te) Теллурофен C4H4Te Тетрабромид теллура (TeBr4) Тетрагидроортотеллурат калия K2H4TeO6 Тетраиодид теллура (TeI4) Тетрафторид теллура (TeF4) Тетрахлорид теллура (TeCl4) Триоксид теллура (TeO3) Трителлурид дикалия (K2Te3) |
| Периодическая система химических элементов Д. И. Менделеева | ||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | |||||||||||||||
| 1 | H | He | ||||||||||||||||||||||||||||||
| 2 | Li | Be | B | C | N | O | F | Ne | ||||||||||||||||||||||||
| 3 | Na | Mg | Al | Si | P | S | Cl | Ar | ||||||||||||||||||||||||
| 4 | K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | ||||||||||||||
| 5 | Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe | ||||||||||||||
| 6 | Cs | Ba | La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn |
| 7 | Fr | Ra | Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Uut | Fl | Uup | Lv | Uus | Uuo |
| 8 | Uue | Ubn | Ubu | Ubb | Ubt | Ubq | Ubp | Ubh | ||||||||||||||||||||||||
теллур википедия, теллур харьков, теллур элемент, теллурий, теллурий фото, теллурит, теллурия, теллурия сорокин, теллурия сорокин скачать, теллурократия
Теллур Информацию О
Oткрытие теллура (англ. Tellurium, нем. Tellur, франц. Tellure) относится к началу расцвета химико-аналитических исследований во второй половине XVIII в. К тому времени в Австрии в области Семигорье (Трансильвания) была найдена новая золотосодержашая руда. Ее называли тогда парадоксальное золото (Aurum paradoxicum), белое золото (Aurum album), проблематичное золото (Aurum problematicum), так как минералоги ничего не знали о природе этой руды, горняки же считали, что она содержит висмут или сурьму. В 1782 г. Мюллер (впоследствии барон Рейхенштейн), горный инспектор в Семигорье, исследовал руду и выделил из нее, как он полагал, новый металл. Чтобы удостовериться в своем открытии, Мюллер послал пробу "металла" шведскому химику-аналитику Бергману. Бергман, тогда уже тяжело больной, начал исследование, но успел установить лишь то, что новый металл отличается по химическим свойствам от сурьмы. Последовавшая вскоре смерть Бергмана прервала исследования и, прошло более 16 лет, прежде чем они возобновились. Тем временем в 1786 г. профессор ботаники и химии университета в Пеште Китаибель выделил из минерала верлита (содержащего теллуриды серебра, железа и висмута) какой-то металл, который он счел до тех пор неизвестным. Китаибель составил описание нового металла, но не опубликовал его, а лишь разослал некоторым ученым. Так оно попало к венскому минералогу Эстнеру, который познакомил с ним Клапрота. Последний дал благоприятный отзыв о работе Китаибеля, но существование нового металла пока еще не было окончательно подтверждено. Клапрот продолжил исследования Китаибеля и в результате их полностью устранил всякие сомнения. В январе 1798 г. он выступил с сообщением перед Берлинской академией наук об открытии им в трансильванском "белом золоте" особого металла (!), который получен "от матери земли" и назван поэтому теллуром (Tellur) от слова tellus земля (планета). И действительно, первые десятилетия XIX в. теллур причисляли к металлам. В 1832 r. Берцелиус обратил внимание на сходство теллура с селеном и серой (на что делались указания и раньше), после чего теллур причислили к металлоидам (по номенклатуре Берцелиуса). В русской химической литературе начала XIX в. новый эламент называли теллуром, теллурием, теллюром, теллюрием; после появления учебника химии Гесса укоренилось название теллур.
17,91 кДж/моль
49,8 кДж/моль
гексагональная
a =4,457 c =5,929
(300 K) 14,3 Вт/(м·К)
Встречается самородный теллур и вместе с селеном и серой (японская теллуристая сера содержит 0,17 % Те и 0,06 % Se).
Типы месторождений
Большая часть упомянутых минералов развита в низкотемпературных золото-серебряных месторождениях, где они обычно выделяются после основной массы сульфидов совместно с самородным золотом, сульфосолями серебра, свинца, а также с минералами висмута . Несмотря на развитие большого числа теллуровых минералов, главная масса теллура, извлекаемого промышленностью, входит в состав сульфидов других металлов. В частности, теллур в несколько меньшей степени, чем селен , входит в состав халькопирита медно-никелевых месторождений магматического происхождения, а также халькопирита, развитого в медноколчеданных гидротермальных месторождениях. Теллур находится также в составе пирита , халькопирита, молибденита и галенита месторождений порфировых медных руд, полиметаллических месторождений алтайского типа, галенита свинцово-цинковых месторождений, связанных со скарнами, сульфидно-кобальтовых, сурьмяно-ртутных и некоторых других. Содержание теллура в молибдените колеблется в пределах 8-53 г/т, в халькопирите 9-31 г/т, в пирите - до 70 г/т.
Получение
Химические свойства
В химических соединениях теллур проявляет степени окисления –2; +2; +4; +6. Является аналогом серы и селена , но химически менее активен, чем сера. Растворяется в щелочах, поддается действию азотной и серной кислот, но в разбавленной соляной кислоте растворяется слабо. С водой металлический теллур начинает реагировать при 100 °C .
С кислородом образует соединения TeO, TeO 2 , TeO 3 . В виде порошка окисляется на воздухе даже при комнатной температуре, образуя оксид TeO 2 . При нагреве на воздухе сгорает, образуя TeO 2 - прочное соединение, обладающее меньшей летучестью, чем сам теллур. Это свойство используется для очистки теллура от оксидов, которые восстанавливают проточным водородом при температуре 500-600 °C . Диоксид теллура плохо растворим в воде, хорошо - в кислых и щелочных растворах .
В расплавленном состоянии теллур довольно инертен, поэтому в качестве контейнерных материалов при его плавке применяют графит и кварц.
Теллур образует соединение с водородом при нагревании, легко реагирует с галогенами, взаимодействует с серой, фосфором и металлами. При взаимодействии с концентрированной серной кислотой образует сульфит . Образует слабые кислоты: теллурводородную (H 2 Te), теллуристую (H 2 TeO 3) и теллуровую (H 6 TeO 6), большинство солей которых плохо растворимы в воде .
Изотопы
Применение
Сплавы
Теллур применяется в производстве сплавов свинца с повышенной пластичностью и прочностью (применяемых, например, при производстве кабелей). При введении 0,05 % теллура потери свинца на растворение под воздействием серной кислоты снижаются в 10 раз, и это используется при производстве свинцово-кислотных аккумуляторов . Так же важно то обстоятельство, что легированный теллуром свинец при обработке пластической деформацией не разупрочняется, и это позволяет вести технологию изготовления токоотводов аккумуляторных пластин методом холодной высечки и значительно увеличить срок службы и удельные характеристики аккумулятора.
В составе сплава CZT (теллурид кадмия-цинка, CdZnTe) применяется в производстве детекторов рентгеновского и гамма- излучений, которые работают при комнатной температуре.
Термоэлектрические материалы
Также велика его роль в производстве полупроводниковых материалов и, в частности, теллуридов свинца , висмута , сурьмы , цезия . Очень важное значение в ближайшие годы приобретёт производство теллуридов лантаноидов, их сплавов и сплавов с селенидами металлов для производства термоэлектрогенераторов с весьма высоким (до 72-78 %) КПД , что позволит применить их в энергетике и в автомобильной промышленности.
Так, например, недавно обнаружена очень высокая термо-ЭДС в теллуриде марганца (500 мкВ/К) и в его сочетании с селенидами висмута, сурьмы и лантаноидов , что позволяет не только достичь весьма высокого КПД в термогенераторах, но и осуществить уже в одной ступени полупроводникового холодильника охлаждение вплоть до области криогенных (температурный уровень жидкого азота) температур и даже ниже. Лучшим материалом на основе теллура для производства полупроводниковых холодильников в последние годы явился сплав теллура, висмута и цезия , который позволил получить рекордное охлаждение до −237 °C. В то же время, как термоэлектрический материал, перспективен сплав теллур-селен (70 % селена), который имеет коэффициент термо-ЭДС около 1200 мкВ/К.
Узкозонные полупроводники
Совершенно исключительное значение также получили сплавы КРТ (кадмий - -теллур), которые обладают фантастическими характеристиками для обнаружения излучения от стартов ракет и наблюдения за противником из космоса через атмосферные окна (не имеет значения облачность). КРТ является одним из наиболее дорогих материалов в современной электронной промышленности.
Высокотемпературная сверхпроводимость
Ряд систем, имеющих в своем составе теллур, недавно обнаружили существование в них трёх (возможно, четырёх) фаз, сверхпроводимость в которых не исчезает при температуре несколько выше температуры кипения жидкого азота .
Производство резины
Отдельной областью применения теллура является его использование в процессе вулканизации каучука .
Производство халькогенидных стёкол
Теллур используется при варке специальных марок стекла (где он применяется в виде диоксида), специальные стёкла, легированные редкоземельными металлами , применяются в качестве активных тел оптических квантовых генераторов .
Кроме того, некоторые стёкла на основе теллура являются полупроводниками, это свойство находит применение в электронике.
Специальные сорта теллурового стекла (достоинство таких стёкол - прозрачность, легкоплавкость и электропроводность), применяются в конструировании специальной химической аппаратуры (реакторов).
Ограниченное применение теллур находит для производства ламп с его парами - они имеют спектр, очень близкий к солнечному.
CD-RW
Сплав теллура применяется в перезаписываемых компакт-дисках (в частности, фирмы Mitsubishi Chemical Corporation марки «Verbatim») для создания деформируемого отражающего слоя.
Биологическая роль
Физиологическое действие
Теллур и его летучие соединения токсичны. Попадание в организм вызывает тошноту , бронхиты , пневмонию . ПДК в воздухе колеблется для различных соединений 0,007-0,01 мг/м³, в воде 0,001-0,01 мг/л. Канцерогенность теллура не подтверждена .
При отравлениях теллур выводится из организма в виде отвратительно пахнущих летучих теллурорганических соединений - алкилтеллуридов , в основном диметилтеллурида (CH 3) 2 Te. Их запах напоминает запах чеснока , поэтому при попадании в организм даже малых количеств теллура выдыхаемый человеком воздух приобретает этот запах, что является важным симптомом отравления теллуром .
Напишите отзыв о статье "Теллур"
Примечания
- Michael E. Wieser, Norman Holden, Tyler B. Coplen, John K. Böhlke, Michael Berglund, Willi A. Brand, Paul De Bièvre, Manfred Gröning, Robert D. Loss, Juris Meija, Takafumi Hirata, Thomas Prohaska, Ronny Schoenberg, Glenda O’Connor, Thomas Walczyk, Shige Yoneda, Xiang‑Kun Zhu. (англ.) // Pure and Applied Chemistry . - 2013. - Vol. 85 , no. 5 . - P. 1047-1078 . - DOI :10.1351/PAC-REP-13-03-02 .
- (англ.) . WebElements. Проверено 5 августа 2010.
- Leddicotte, G. W. (1961),
, Nuclear science series, Subcommittee on Radiochemistry, National Academy of Sciences-National Research Council, с. 5,
- Редкол.:Зефиров Н. С. (гл. ред.). Химическая энциклопедия: в 5 т. - Москва: Советская энциклопедия, 1995. - Т. 4. - С. 514. - 639 с. - 20 000 экз. - ISBN 5-85270-039-8.
- Глинка Н. Л. Общая химия. - М .: «Химия», 1977, переработанное. - С. 395. - 720 с.
- Теллур - статья из Большой советской энциклопедии
- G. Audi, O. Bersillon, J. Blachot and A. H. Wapstra (2003). «». Nuclear Physics A 729 : 3–128. DOI :10.1016/j.nuclphysa.2003.11.001 . Bibcode : .
- Изотоп теллур-123 считался радиоактивным (β − -активным с периодом полураспада 6·10 14 лет), однако после дополнительных измерений он был признан стабильным в пределах чувствительности эксперимента.
- 2,2 квадриллиона лет - по длинной шкале .
- . International Programme on Chemical Safety (28 января 1998). Проверено 12 января 2007. .
- Wright, PL (1966). «». AJP – Legacy 211 (1): 6–10. PMID 5911055 .
- (1989) «Tellurium-intoxication». Klinische Wochenschrift 67 (22): 1152–5. DOI :10.1007/BF01726117 . PMID 2586020 .
- Taylor, Andrew (1996). «Biochemistry of tellurium». Biological Trace Element Research 55 (3): 231–239. DOI :10.1007/BF02785282 . PMID 9096851 .
Ссылки
| Периодическая система химических элементов Д. И. Менделеева | ||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Te | ||||||||||||||||||||||||||||||||
| Щёлочноземельные металлы | ||||||||||||||||||||||||||||||||
Отрывок, характеризующий Теллур
Ввечеру Наполеон между двумя распоряжениями – одно о том, чтобы как можно скорее доставить заготовленные фальшивые русские ассигнации для ввоза в Россию, и другое о том, чтобы расстрелять саксонца, в перехваченном письме которого найдены сведения о распоряжениях по французской армии, – сделал третье распоряжение – о причислении бросившегося без нужды в реку польского полковника к когорте чести (Legion d"honneur), которой Наполеон был главою.Qnos vult perdere – dementat. [Кого хочет погубить – лишит разума (лат.) ]
Русский император между тем более месяца уже жил в Вильне, делая смотры и маневры. Ничто не было готово для войны, которой все ожидали и для приготовления к которой император приехал из Петербурга. Общего плана действий не было. Колебания о том, какой план из всех тех, которые предлагались, должен быть принят, только еще более усилились после месячного пребывания императора в главной квартире. В трех армиях был в каждой отдельный главнокомандующий, но общего начальника над всеми армиями не было, и император не принимал на себя этого звания.
Чем дольше жил император в Вильне, тем менее и менее готовились к войне, уставши ожидать ее. Все стремления людей, окружавших государя, казалось, были направлены только на то, чтобы заставлять государя, приятно проводя время, забыть о предстоящей войне.
После многих балов и праздников у польских магнатов, у придворных и у самого государя, в июне месяце одному из польских генерал адъютантов государя пришла мысль дать обед и бал государю от лица его генерал адъютантов. Мысль эта радостно была принята всеми. Государь изъявил согласие. Генерал адъютанты собрали по подписке деньги. Особа, которая наиболее могла быть приятна государю, была приглашена быть хозяйкой бала. Граф Бенигсен, помещик Виленской губернии, предложил свой загородный дом для этого праздника, и 13 июня был назначен обед, бал, катанье на лодках и фейерверк в Закрете, загородном доме графа Бенигсена.
В тот самый день, в который Наполеоном был отдан приказ о переходе через Неман и передовые войска его, оттеснив казаков, перешли через русскую границу, Александр проводил вечер на даче Бенигсена – на бале, даваемом генерал адъютантами.
Был веселый, блестящий праздник; знатоки дела говорили, что редко собиралось в одном месте столько красавиц. Графиня Безухова в числе других русских дам, приехавших за государем из Петербурга в Вильну, была на этом бале, затемняя своей тяжелой, так называемой русской красотой утонченных польских дам. Она была замечена, и государь удостоил ее танца.
Борис Друбецкой, en garcon (холостяком), как он говорил, оставив свою жену в Москве, был также на этом бале и, хотя не генерал адъютант, был участником на большую сумму в подписке для бала. Борис теперь был богатый человек, далеко ушедший в почестях, уже не искавший покровительства, а на ровной ноге стоявший с высшими из своих сверстников.
В двенадцать часов ночи еще танцевали. Элен, не имевшая достойного кавалера, сама предложила мазурку Борису. Они сидели в третьей паре. Борис, хладнокровно поглядывая на блестящие обнаженные плечи Элен, выступавшие из темного газового с золотом платья, рассказывал про старых знакомых и вместе с тем, незаметно для самого себя и для других, ни на секунду не переставал наблюдать государя, находившегося в той же зале. Государь не танцевал; он стоял в дверях и останавливал то тех, то других теми ласковыми словами, которые он один только умел говорить.
При начале мазурки Борис видел, что генерал адъютант Балашев, одно из ближайших лиц к государю, подошел к нему и непридворно остановился близко от государя, говорившего с польской дамой. Поговорив с дамой, государь взглянул вопросительно и, видно, поняв, что Балашев поступил так только потому, что на то были важные причины, слегка кивнул даме и обратился к Балашеву. Только что Балашев начал говорить, как удивление выразилось на лице государя. Он взял под руку Балашева и пошел с ним через залу, бессознательно для себя расчищая с обеих сторон сажени на три широкую дорогу сторонившихся перед ним. Борис заметил взволнованное лицо Аракчеева, в то время как государь пошел с Балашевым. Аракчеев, исподлобья глядя на государя и посапывая красным носом, выдвинулся из толпы, как бы ожидая, что государь обратится к нему. (Борис понял, что Аракчеев завидует Балашеву и недоволен тем, что какая то, очевидно, важная, новость не через него передана государю.)
Но государь с Балашевым прошли, не замечая Аракчеева, через выходную дверь в освещенный сад. Аракчеев, придерживая шпагу и злобно оглядываясь вокруг себя, прошел шагах в двадцати за ними.
Пока Борис продолжал делать фигуры мазурки, его не переставала мучить мысль о том, какую новость привез Балашев и каким бы образом узнать ее прежде других.
В фигуре, где ему надо было выбирать дам, шепнув Элен, что он хочет взять графиню Потоцкую, которая, кажется, вышла на балкон, он, скользя ногами по паркету, выбежал в выходную дверь в сад и, заметив входящего с Балашевым на террасу государя, приостановился. Государь с Балашевым направлялись к двери. Борис, заторопившись, как будто не успев отодвинуться, почтительно прижался к притолоке и нагнул голову.
Государь с волнением лично оскорбленного человека договаривал следующие слова:
– Без объявления войны вступить в Россию. Я помирюсь только тогда, когда ни одного вооруженного неприятеля не останется на моей земле, – сказал он. Как показалось Борису, государю приятно было высказать эти слова: он был доволен формой выражения своей мысли, но был недоволен тем, что Борис услыхал их.
– Чтоб никто ничего не знал! – прибавил государь, нахмурившись. Борис понял, что это относилось к нему, и, закрыв глаза, слегка наклонил голову. Государь опять вошел в залу и еще около получаса пробыл на бале.
Борис первый узнал известие о переходе французскими войсками Немана и благодаря этому имел случай показать некоторым важным лицам, что многое, скрытое от других, бывает ему известно, и через то имел случай подняться выше во мнении этих особ.
Неожиданное известие о переходе французами Немана было особенно неожиданно после месяца несбывавшегося ожидания, и на бале! Государь, в первую минуту получения известия, под влиянием возмущения и оскорбления, нашел то, сделавшееся потом знаменитым, изречение, которое самому понравилось ему и выражало вполне его чувства. Возвратившись домой с бала, государь в два часа ночи послал за секретарем Шишковым и велел написать приказ войскам и рескрипт к фельдмаршалу князю Салтыкову, в котором он непременно требовал, чтобы были помещены слова о том, что он не помирится до тех пор, пока хотя один вооруженный француз останется на русской земле.
На другой день было написано следующее письмо к Наполеону.
«Monsieur mon frere. J"ai appris hier que malgre la loyaute avec laquelle j"ai maintenu mes engagements envers Votre Majeste, ses troupes ont franchis les frontieres de la Russie, et je recois a l"instant de Petersbourg une note par laquelle le comte Lauriston, pour cause de cette agression, annonce que Votre Majeste s"est consideree comme en etat de guerre avec moi des le moment ou le prince Kourakine a fait la demande de ses passeports. Les motifs sur lesquels le duc de Bassano fondait son refus de les lui delivrer, n"auraient jamais pu me faire supposer que cette demarche servirait jamais de pretexte a l"agression. En effet cet ambassadeur n"y a jamais ete autorise comme il l"a declare lui meme, et aussitot que j"en fus informe, je lui ai fait connaitre combien je le desapprouvais en lui donnant l"ordre de rester a son poste. Si Votre Majeste n"est pas intentionnee de verser le sang de nos peuples pour un malentendu de ce genre et qu"elle consente a retirer ses troupes du territoire russe, je regarderai ce qui s"est passe comme non avenu, et un accommodement entre nous sera possible. Dans le cas contraire, Votre Majeste, je me verrai force de repousser une attaque que rien n"a provoquee de ma part. Il depend encore de Votre Majeste d"eviter a l"humanite les calamites d"une nouvelle guerre.
Je suis, etc.
(signe) Alexandre».
[«Государь брат мой! Вчера дошло до меня, что, несмотря на прямодушие, с которым соблюдал я мои обязательства в отношении к Вашему Императорскому Величеству, войска Ваши перешли русские границы, и только лишь теперь получил из Петербурга ноту, которою граф Лористон извещает меня, по поводу сего вторжения, что Ваше Величество считаете себя в неприязненных отношениях со мною, с того времени как князь Куракин потребовал свои паспорта. Причины, на которых герцог Бассано основывал свой отказ выдать сии паспорты, никогда не могли бы заставить меня предполагать, чтобы поступок моего посла послужил поводом к нападению. И в действительности он не имел на то от меня повеления, как было объявлено им самим; и как только я узнал о сем, то немедленно выразил мое неудовольствие князю Куракину, повелев ему исполнять по прежнему порученные ему обязанности. Ежели Ваше Величество не расположены проливать кровь наших подданных из за подобного недоразумения и ежели Вы согласны вывести свои войска из русских владений, то я оставлю без внимания все происшедшее, и соглашение между нами будет возможно. В противном случае я буду принужден отражать нападение, которое ничем не было возбуждено с моей стороны. Ваше Величество, еще имеете возможность избавить человечество от бедствий новой войны.
(подписал) Александр». ]
13 го июня, в два часа ночи, государь, призвав к себе Балашева и прочтя ему свое письмо к Наполеону, приказал ему отвезти это письмо и лично передать французскому императору. Отправляя Балашева, государь вновь повторил ему слова о том, что он не помирится до тех пор, пока останется хотя один вооруженный неприятель на русской земле, и приказал непременно передать эти слова Наполеону. Государь не написал этих слов в письме, потому что он чувствовал с своим тактом, что слова эти неудобны для передачи в ту минуту, когда делается последняя попытка примирения; но он непременно приказал Балашеву передать их лично Наполеону.
Выехав в ночь с 13 го на 14 е июня, Балашев, сопутствуемый трубачом и двумя казаками, к рассвету приехал в деревню Рыконты, на французские аванпосты по сю сторону Немана. Он был остановлен французскими кавалерийскими часовыми.
Французский гусарский унтер офицер, в малиновом мундире и мохнатой шапке, крикнул на подъезжавшего Балашева, приказывая ему остановиться. Балашев не тотчас остановился, а продолжал шагом подвигаться по дороге.
Унтер офицер, нахмурившись и проворчав какое то ругательство, надвинулся грудью лошади на Балашева, взялся за саблю и грубо крикнул на русского генерала, спрашивая его: глух ли он, что не слышит того, что ему говорят. Балашев назвал себя. Унтер офицер послал солдата к офицеру.
Не обращая на Балашева внимания, унтер офицер стал говорить с товарищами о своем полковом деле и не глядел на русского генерала.
Необычайно странно было Балашеву, после близости к высшей власти и могуществу, после разговора три часа тому назад с государем и вообще привыкшему по своей службе к почестям, видеть тут, на русской земле, это враждебное и главное – непочтительное отношение к себе грубой силы.
Солнце только начинало подниматься из за туч; в воздухе было свежо и росисто. По дороге из деревни выгоняли стадо. В полях один за одним, как пузырьки в воде, вспырскивали с чувыканьем жаворонки.
Балашев оглядывался вокруг себя, ожидая приезда офицера из деревни. Русские казаки, и трубач, и французские гусары молча изредка глядели друг на друга.
Французский гусарский полковник, видимо, только что с постели, выехал из деревни на красивой сытой серой лошади, сопутствуемый двумя гусарами. На офицере, на солдатах и на их лошадях был вид довольства и щегольства.
Это было то первое время кампании, когда войска еще находились в исправности, почти равной смотровой, мирной деятельности, только с оттенком нарядной воинственности в одежде и с нравственным оттенком того веселья и предприимчивости, которые всегда сопутствуют началам кампаний.
Французский полковник с трудом удерживал зевоту, но был учтив и, видимо, понимал все значение Балашева. Он провел его мимо своих солдат за цепь и сообщил, что желание его быть представленну императору будет, вероятно, тотчас же исполнено, так как императорская квартира, сколько он знает, находится недалеко.
Они проехали деревню Рыконты, мимо французских гусарских коновязей, часовых и солдат, отдававших честь своему полковнику и с любопытством осматривавших русский мундир, и выехали на другую сторону села. По словам полковника, в двух километрах был начальник дивизии, который примет Балашева и проводит его по назначению.
Солнце уже поднялось и весело блестело на яркой зелени.
Только что они выехали за корчму на гору, как навстречу им из под горы показалась кучка всадников, впереди которой на вороной лошади с блестящею на солнце сбруей ехал высокий ростом человек в шляпе с перьями и черными, завитыми по плечи волосами, в красной мантии и с длинными ногами, выпяченными вперед, как ездят французы. Человек этот поехал галопом навстречу Балашеву, блестя и развеваясь на ярком июньском солнце своими перьями, каменьями и золотыми галунами.
Балашев уже был на расстоянии двух лошадей от скачущего ему навстречу с торжественно театральным лицом всадника в браслетах, перьях, ожерельях и золоте, когда Юльнер, французский полковник, почтительно прошептал: «Le roi de Naples». [Король Неаполитанский.] Действительно, это был Мюрат, называемый теперь неаполитанским королем. Хотя и было совершенно непонятно, почему он был неаполитанский король, но его называли так, и он сам был убежден в этом и потому имел более торжественный и важный вид, чем прежде. Он так был уверен в том, что он действительно неаполитанский король, что, когда накануне отъезда из Неаполя, во время его прогулки с женою по улицам Неаполя, несколько итальянцев прокричали ему: «Viva il re!», [Да здравствует король! (итал.) ] он с грустной улыбкой повернулся к супруге и сказал: «Les malheureux, ils ne savent pas que je les quitte demain! [Несчастные, они не знают, что я их завтра покидаю!]
Но несмотря на то, что он твердо верил в то, что он был неаполитанский король, и что он сожалел о горести своих покидаемых им подданных, в последнее время, после того как ему ведено было опять поступить на службу, и особенно после свидания с Наполеоном в Данциге, когда августейший шурин сказал ему: «Je vous ai fait Roi pour regner a maniere, mais pas a la votre», [Я вас сделал королем для того, чтобы царствовать не по своему, а по моему.] – он весело принялся за знакомое ему дело и, как разъевшийся, но не зажиревший, годный на службу конь, почуяв себя в упряжке, заиграл в оглоблях и, разрядившись как можно пестрее и дороже, веселый и довольный, скакал, сам не зная куда и зачем, по дорогам Польши.